Forskere ved Københavns Universitet har utviklet en kunstig mage og tynntarm som kan brukes til forskning rundt probiotika og sykdomsbehandling. Første forsøk er foretatt med bakteriebekjempende virus.
Forbruket av antibiotika og sink i landbruket og blant mennesker skal minskes. Det er både danske og europeiske myndigheter enige om, og derfor trengs det alternativer, slik at verken vi eller grisene blir syke.
Noen av disse alternativene blir i øyeblikket testet i en kunstig tynntarm på Københavns Universitet.
På den måten er det nemlig mulig å gjennomføre større studier in vitro, og dermed unngå de etiske problemene som kan oppstå hvis man vil ha effektive tester av for eksempel prebiotika og probiotika.
Selv om det er mulig at begge kan være velegnede alternativer eller supplementer, kan det nemlig være vanskelig å teste dem grundig. Årsaken er at de mest velegnede testene i praksis ville kreve at forsøkspersonen eller -dyret får tilført sykdomsfremkallende bakterier, for at man deretter kan se om de blir fjernet effektivt med det testede stoffet.
Og selv om barrierene er færre når det gjelder tester på dyr, ligger det her noen begrensninger i at mikrobiotaene – det vil si tarmfloraen – til mus og mennesker er vidt forskjellige, forteller postdoc Tomasz Cieplak ved Institut for Fødevarevidenskab på Københavns Universitet.
– Det er dyrt og vanskelig i det hele tatt å forske på bakterier på mennesker, for folks mikrobiota varierer veldig, så det er også vanskelig å reprodusere resultatene. Det samme gjelder for så vidt for dyr, og sammenligningen mellom dyr og mennesker er heller ikke alltid optimal, sier han.
– Derfor er det mening i å teste så mye som mulig in vitro, og det kan la seg gjøre i vår kunstige mage og tynntarm, hvor det også er enklere å sterilisere miljøet og bytte ut infiserte deler.
- Antibiotika-resistens: Norske forskere kan løse en av menneskehetens største utfordringer
Maskin med fem mager og tarmer
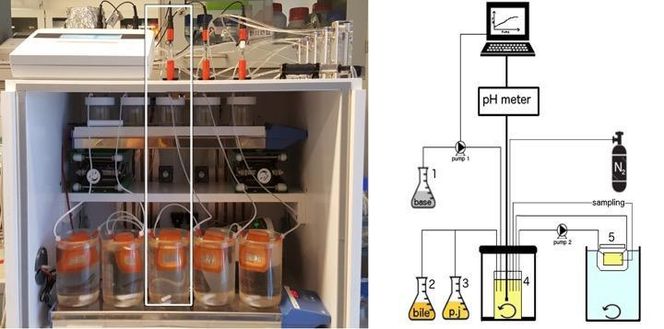
Som et ledd i sitt ph.d.-prosjekt har Tomasz Cieplak bygget en modell som kan simulere passasjen gjennom mage og tynntarm hos fem ‘individer’ samtidig.

.jpg)
I modellen kan man simulere faktorer som pH, som endrer seg mye gjennom den øvre delen av mage-tarm-kanalen, og effekten av fordøyelsesenzymer og gallesalter. Dessuten kan gallesaltene re-absorberes ved hjelp dialysemembraner, slik at mikroorganismene som testes i modellen utsettes for fysiologisk relevante forhold.
Ifølge Tomasz Cieplak har utfordringen vært å gjøre ‘tarmen’ så kompakt som mulig. Til gjengjeld er det mulig å teste svært små mengder bakterier i tarmen, og det kan være en fordel, siden noen blandinger – så som karbohydrater fra brystmelk – er svært dyre.
Instituttet har i første omgang nylig kartlagt ‘tarmens’ effektivitet i et forsøk utført i samarbeid med den amerikanske biotek-bedriften Intralytix, hvor det ble undersøkt om bakteriofagene deres kunne drepe den sykdomsfremkallende bakterien E.coli, hvis de blir gitt som en forebyggende blanding.
- Ninjapolymerer: Kan knerte multiresistente bakterier
Bakteriofager spiser bakteriene
Bakteriofager er virus som angriper helt bestemte bakterier for å bruke dem til å reprodusere og spre seg i. De finnes i store mengder i vår egen mikrobiota, og der spiller de en viktig rolle med hensyn til balansen av mikrobiotaen i tarmen vår, siden deres snyltende oppgave sørger for at bakterien dør underveis.
Derfor kan de også samles inn gjennom filtrering av avføringsprøver, og ved å få tak i de helt riktige – i dette tilfelle de bakteriofagene som angriper E.coli – kan man i prinsippet formere dem i rikelige mengder og gi dem som behandling mot mageproblemer som er forårsaket av nettopp E.coli.


Det er i hvert fall denne ideen som forskerne jobber med, og som den kunstige tynntarmen har testet, forteller professor Dennis Sandris Nielsen på instituttet.
– Vi har her for første gang vist at en blanding med tre bakteriofager er like effektiv til å drepe E.coli som antibiotika i et system som simulerer tynntarmen vår, sier Dennis Sandris Nielsen.
– Det er jo veldig interessant, fordi bakteriofager er vertsspesifikke, og bare angriper én bakteriestamme. Det innebærer at de – i motsetning til antibiotika, som treffer bredt – lar de gode bakteriene i tarmen leve videre, sier han.
- Les også: Her er teknologiene som kan forhindre at antibiotikaresistens blir den verste helsekatastrofen siden svartedauden (TU Ekstra)
Skal erstatte antibiotika og sink
Men Dennis Sandris Nielsen understreker at forsøkene nå også må kunne reproduseres i først mus og deretter i mennesker. Og selv om det lykkes å få effektive blandinger med bakteriofager på markedet, vil det innebære at disse blandingene sannsynligvis må byttes ut litt oftere i hyllene enn tradisjonell antibiotika.
Årsaken er det naturlige seleksjonspresset som gjør at bakteriene vil forsøke å mutere, slik at viruset ikke lengre kan gjenkjenne dem.
– Det betyr at du – i motsetning til de mer bredspektrede antibiotikaene – er nødt til hele tiden å følge med og isolere nye bakteriofager som har klart å slå bakterien i kappløpet, understreker Dennis Sandris Nielsen.
Med denne vellykkede erfaringen i bagasjen, at tynntarmen med fordel kan brukes til denne typen forskning, kaster KU-forskerne seg nå over flere lignende prosjekter.
Ifølge Tomasz Cieplak samarbeider forskerne med flere bedrifter og universiteter om utvikling av pre- og probiotika.
Instituttet har blant annet, sammen med ingrediensbedriften Chr. Hansen, fått midler fra den danske Innovationsfonden til et prosjekt hvor Tomasz Cieplak skal bygge en kunstig grisetarm, hvor det kan testes mulige alternativer til antibiotika og sink, som vil få sterke bruksbegrensninger i løpet av de neste årene.
– Dette blir også et kjempeprosjekt, men vi har fremdeles ikke begynt på det, sier han.
Artikkelen ble først publisert på Ing.dk
- Smarthuslandsbyen klikket: Etter tre år med problemer har Aron endelig fått et «dummere» hus






