De ørsmå plageåndene har vist seg å være mye verre å få has på enn vi har trodd i en verden som har flommet over av potente antibiotika.
Det skyldes først og fremst vår egen uvettige bruk av medisinene, og vi kan ikke si at vi ikke ble advart. Allerede i sitt Nobellforedrag i 1945 sa Alexander Flemming, som oppdaget Penicillin i 1928, at vi måtte være forsiktig med bruken så bakteriene ikke utviklet resistens.
Flemming skjønte hvordan det kunne gå hvis Darwins «survival of the fittest» fikk utfolde seg i hurtigfilm.
Men vi har ikke hørt på advarselen fra Nobelprisvinneren. Både folk og fe har fått rikelig med antibiotika. Og det fortsetter.
Et av stoffene vi kan kalle siste skanse antibiotika, slike som meropenem, som vi i Norge bare benytter om alt annet feiler, selges til hvem som helst over disk i India. Det er allerede bakteriestammer som har utviklet resistens mot dette legemiddelet, og med de reisevaner folk har i dag kan slike raskt flytte seg over hele verden.
Kritisk situasjon
I dag er situasjonen særdeles kritisk. Mange bakteriestammer er omtrent umulige å få has på, og det blir stadig verre. Det jaktes på nye antibiotika, og det er noen i den såkalte pipelinen, men faren for at det går samme vei med dem er stor.
Blir det verre kan det bli vanskelig å utføre selv små operasjoner. Den minste infeksjon i et sår kan medføre stor fare. Avansert kirurgi og organtransplantasjoner kan være forbundet med livsfare og selv små rifter i huden kan ende fatalt. Det er vanskelig å sette seg inn i for mennesker som lever i dag. De færreste husker hvordan det var før antibiotika, selv om situasjonen da ikke var så ille som det kan bli i dag om antibiotika blir virkningsløst. Folk reiste ikke rundt og tok med seg bakterier og sykdommer fra fjern og nær som vi gjør nå.
Økonomen Jim o’Neil har sagt at om vi ikke løser dette problemet vil det dø flere av infeksjoner i 2050 enn av kreft, til en kostnad av nesten 10 000 milliarder kroner.
Kanskje en av løsningene er svært nær, og norsk.


Stripper av rustningen
Det er liten tvil om at vi trenger nye potente virkestoffer fra naturen. Men samtidig som nye antibiotika må knekke de farlige bakteriene, bør de skåne de gode.
Til nå har vi lett høyt og lavt etter nye virkestoffer i naturen, men de lavthengene kirsebærene er plukket for lengst. Det er åpenlyst at det trengs nytenkning. Og tenkt nytt er akkurat det professor Pål Rongved og siv. ing. i kjemi, dr. Ove Alexander Åstrand ved farmasøytisk institutt ved Universitetet i Oslo har gjort.
Sammen med mange medarbeidere har de utviklet et stoff som ikke er giftig, hverken for bakterier eller mennesker, men som har den virkning at det bokstavelig talt kler resistensen av bakteriene. Resultatet er at tradisjonell antibiotika virker igjen. Det kan høres ut som medisinens våte drøm, men i løpet av noen år vil det vise seg om det er det.

De første dyreforsøkene virker lovende. Svært lovende. Mus smittet med dødelige resistente bakterier blir friske når de får en dose av stoffet forskerne har utviklet sammen med den «uvirksomme» antibiotikaen. Uten virkestoffet hadde det vær kroken på døra for de små gnagerne.
Professor Rongved er ingen nykommer. Han har 22 år bak seg som organisk kjemiker i legemiddelbransjen og jobbet i sin tid sammen med den berømte Sintef-forskeren John Ugelstad som fant opp de monodisperse kulene. Her lærte han også betydningen av patentering, og det nye stoffet de har funnet er behørig patentert.


Da de to kjemiforskerne begynte å lete etter nye virksomme molekyler var tanken å finne en ny gruppe stoffer som kunne drepe kreftceller. Under sitt doktorgradsarbeid og post.doc-periode lagde Åstrand og gruppen rundt 250 stoffer og mange varianter av den for å finjustere egenskapene. De begynte med stoffer som har overflater med såkalte metall-kelatorer, som kan minne om molekylære krabbeklør. Men de fungerte ikke som de håpet – mot kreft. I stedet ville de teste stoffet på resistente bakterier, og slike har vi mange av i Tromsø.
Hos professor Ørjan Samuelsen ved K-Res lab, UNN, fikk de tilgang på de farlige bakteriene de trengte. Der har de et nasjonalt ansvar for å oppbevare våre verste mikrobielle fiender på en svært sikker måte til bruk i forskning.
- IBM med ny ploymerteknologi: Kan knerte multiresistente bakterier
Knekker de verste bakteriene
– Vi er omgitt av en rekke farlige resistente bakterier, men noen av de verste er de som opptrer på sykehus. De har vært nesten umulige å bli kvitt. Til denne gruppen hører bakterier som Pseudomonas aeruginosa, E. coli og andre. Det er såkalte Gram-negative bakterier som betyr at de har doble membraner og er ekstra vanskelige å få has på. Utvalget av antibiotika har vært mindre mot denne bakteriegruppen, og nå er det i ferd med å tørke helt opp. Spesielt på sykehus hvor det er mye syke mennesker med nedsatt immunforsvar. Men vi har oppdaget er at de har et svakt punkt, sier Rongved.
Det molekylet forskerne har utviklet har en mekanisme som binder seg til sinkatomene som finnes i svært mange av de resistensmekanismene bakteriene har utviklet.
– Tradisjonelle antibiotika bruker stoffer som kalles betalaktamer, som virker ved å binde seg til enzymene som lager cellemembranen i bakterien. Det er den sammen måten penicillin virket på. I dag er mellom 60 og 70 prosent av
Arbeidet til Rognveds gruppe usedvanlig spennende og oppløftende og kan få en enorm betydning for verdens helse.
Elisabeth Astrup, Nasjonalt folkehelseinstitutt
alle antibiotika basert på betalaktamer, sier Åstrand.
For å kunne tåle ulike antibiotika har mange bakerier utviklet en resistensmekanisme, enzymer som bruker to sinkatomer. Det lille trikset er nok til å gjøre at medisinene ikke virker og et av de verste mekanismene har fått navnet NDM-1 (New Delhi Metallo-betalaktamase 1). Problemet er at stadig flere bakteriegrupper utvikler slike mekanismer basert på en eller to sinkatomer. For å gjøre situasjonen verre kan bakterier også bytte gener med hverandre og på den måten overføre resistens.
– Dette er grunnen til at vi ikke har medisin mot mange av disse Gram-negative bakteriene, sier Rongved.
– Ulike bakterier har utviklet ulik grad av resistens. Noen er resistente mot to til tre antibiotika, andre viser resistens mot åtte til ni og noen få er resistente mot alle kjente antibiotika, sier Åstrand.
- Vi har alle en maksimal levealder: Her er teknologien som kan forlenge den
Tofaktor-behandling
– Bakterier som har utviklet slike sinkbaserte mekanismer, metallo-betalaktamaser, har i praksis en sterk vokter som passer på at antibiotika ikke får virke. Høye doser av antibiotika kan av og til drepe de fleste bakteriene, men ofte overlever noen og da blomstrer infeksjonen opp igjen. Våre data viser at når vi behandler mus med den såkalte sink-kelatoren vi har utviklet, og deretter gir antibiotika, dør alle bakteriene, sier Rongved.
– Vi kan jo ikke hevde at vi løser hele antibiotikaproblemet. Bakterier er ekstremt tilpasningsdyktige, men det ser jo bra ut. Det stoffer vi har utviklet virker på de gramnegative bakteriene, men det er jo flere typer igjen, sier Åsland.
Det de to forskerne mener gir grunn til optimisme er at dette er en tofaktor behandling. Sink-kelatoren de har utviklet er i utgangspunktet helt ufarlig for bakteriene. Det er et hjelpestoff som trengs i tillegg til selve antibiotikaen. Dermed er det to stoffer bakterier må forholde seg til samtidig, og da er det mye vanskeligere for dem å utvikle resistens.
– Bakterier har utviklet seg sammen med organismer som har slått tilbake med det vi kaller antibiotika. Bakteriene har gjennom hundrevis av millioner av år lært seg å håndtere dette. Det de møter nå er noe helt nytt for dem, og det er attpåtil helt ufarlig for dem. Og det er det helt til de får vanlig antibiotika, sier Rongved.
Molekylsnekring

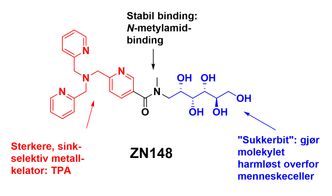
Molekylet forskerne har bygget for å nøytralisere bakterienes resistensmekanisme er delt i tre virkeområder. Den delen som knekker resistensen er en metallbinder som binder seg sterkt til sinkioner, men ikke til andre metaller i kroppen som jern og kalsium. Samtidig er den svært lite toksisk, selv i veldig store konsentrasjoner.
Den andre viktige komponenten er en sukkerdel. Den gjør at stoffet ikke trenger inn i menneskelige celler, men at det trenger inn i ytre membran på Gram-negative bakterier.
Den tredje delen av molekylet er først og fremst en lenke mellom sinkbinderen og sukkerdelen.
Hvis det går som de to forskerne håper kan det nye stoffet bli svært verdifullt, lenge. Fra patentsøknaden har det 20 års beskyttelse, og stoffet er patentsøkt i alle store markeder.
– Vi har en sterk patentsituasjon og det er viktig for alle som investerer, sier Rongved.
Selv om det nye virkestoffet har effekt på gramnegative bakterier har de også grampositive i kikkerten. Det er bakterier med én i stedet for to membraner og mange av de har også utviklet multiresistens, altså resistens mot to eller flere antibiotika, slik som MSRA.
– Det stoffet vi ser på er funnet i Trondheimsfjorden og kan bli en helt ny klasse antibiotika. Det virker mot begge bakterieklassene ved at det virker på arvestoffet i bakteriene og det er giftig for bakteriene. Vi ser på hvordan det også virker i kombinasjon med andre stoffer, sier Rongved.
Den nye antibiotikaen er også giftig for mennesker, men bare i veldig store doser. Tjue ganger større doser enn det som knekker bakteriene.
- Skal ta knekken på den mest aggressive kreften: Større doser stråling på de mest hissige delene av svulsten
Vil ha norsk industri
Fakta
- Forskningen begynte i 2009 for å se hvordan metall-kelatorer kunne påvirke kreftceller.
- I 2013 viste det seg at metall-kelatorer basert på sink hadde en kraftig effekt på resistente bakterier.
- Prosjektet har mottatt støtte fra danske Novo fra 2013 og fra Norges forskningsråd fra 2014.
- I 2016 var rundt 250 ulike varianter av metall-kelatorer sjekket ut for giftighet og andre effekter i mennesker og bakterier.
- I dag har fem såkalte «lead candidates» pekt seg ut og en har spesielt gode egenskaper på alle parameterne som er kontrollert.
- Håper at prosjektet kan gå videre til prekliniske studier om et års tid.
- Det er håp om at behandling med stoffet kan tilbys får de de kliniske studiene er avsluttet på grunn av den potensielt livreddende effekten.
Rongved og Åstrand ønsker at medisinene de utvikler skal produseres i Norge. De mener vi har altfor lite farmasøytisk industri, og at dette kan være en gylden mulighet til å etablere dette. De tror at et sterkt samarbeid mellom UiO og Universitetet i Tromsø kan være et godt fundament i en slik etablering.
– Det er UiO som eier teknologien vi har utviklet, men for å etablere produksjon trenger vi hjelp utenfra. Vi har søkt Olav Thon Foundation om midler og vi håper de kan støtte oss slik som Trond Mohn stiller opp for UiB.
– Det er bare å fryde seg stort over dette! Prosjektet og folkene er et flott eksempel på det vi i Forskningsrådet liker å støtte; forskere som kobler og kombinerer, som vil løse store samfunnsutfordringer og som tenker næringsutvikling. Vi skulle hatt flere Rongved’er, dvs forskere som beveger seg mellom industri og akademia – det er nemlig godt dokumentert at slike er særlig produktive og innovative. At hans forskning er innenfor et så hot område som antibiotikaresistens og knyttet til en stadig mer ambisiøs norsk helsenæring er særlig spennende, sier innovasjonsdirektør i Forskningsrådet, Anne Kjersti Fahlvik.
– Ved Folkehelseinstituttet overvåker vi forekomsten av resistente mikrober i Norge. De forskjellige mikrobene og resistensmekanismene oppfører seg ikke likt, men vi ser at resistens totalt sett øker. Innsatsen for å bremse utviklingen og konsekvensene av resistens foregår på mange fronter; smittevern og restriktiv bruk av allerede eksisterende antibiotika er to vesentlige tiltak, men utvikling av nye behandlingsformer er også helt essensielt for å kunne opprettholde helsetjenestene som i dag. Her er arbeidet til Rognveds gruppe usedvanlig spennende og oppløftende og kan få en enorm betydning for verdens helse, sier lege og seniorrådgiver Elisabeth Astrup i avdeling for resistens- og infeksjonsforebygging ved Nasjonalt folkehelseinstitutt.
Mye gjenstår

Det gjenstår mye forskning og ikke minst uttesting av det nye virkestoffet. Selv om museforsøk viser svært gode resultater skal det flere års uttesting og kliniske forsøk til før det blir et godkjent legemiddel.
– Dette kommer til å bli et etisk dilemma som det ofte er i legemiddelindustrien. Når vi vet at vi kan redde kritisk syke pasienter, skal vi ikke da bruke det? Jeg tror dette vil bli utviklet under det såkalt Fast-Track-regimet før det er godkjent; og hvis det handlet om en kritisk infeksjon av resistente bakterier i egen familie ville jeg ikke nølt i dag. Jeg ville brukt det, sier Rongved.
- Trenger verdens mest sjeldne grunnstoff for å kurere kreft: Norge kan fremstille det kunstig





