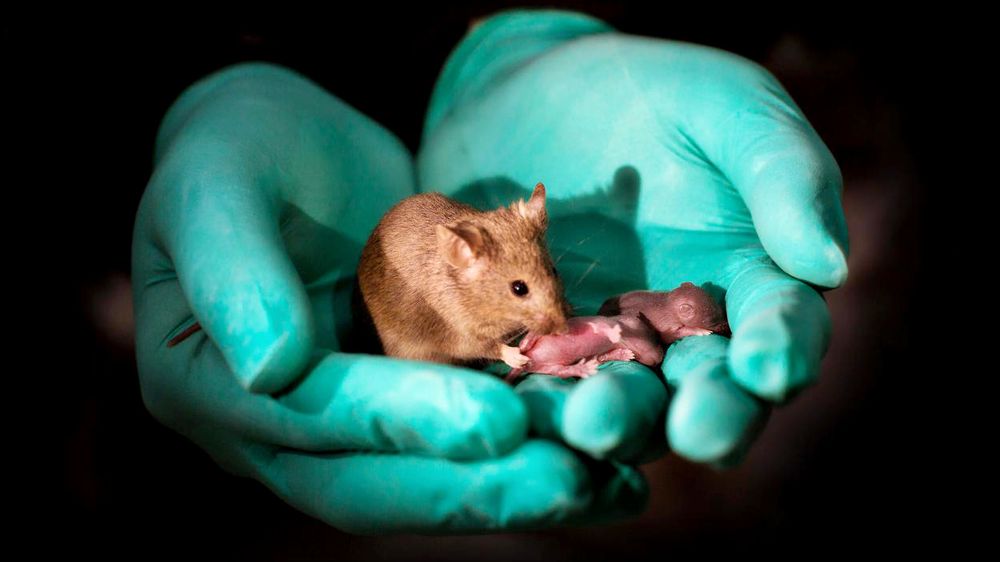
I gamle dager måtte sædcella finne eggcella inne i en kvinne. Nå holder det strengt tatt at de møtes i et prøverør. I fremtiden kan omprogrammerte hudceller gjøre jobben for dem.
Se for deg at folk i absolutt alle aldre kan bli foreldre – fra nyfødte babyer til 100-åringer på gamlehjem. At en sædcelle kan stamme fra en kvinne, en eggcelle fra en mann, og at likekjønnede par derfor kan få barn som er beslektet med begge.


Se også for deg at kvinners biologiske klokke og tidsbegrensede produksjon av egg ikke betyr noe særlig lenger. At folk kan bli foreldre uten å ha samtykket til det eller vite om det i det hele tatt.
Se for deg at assistert befruktning blir et valg mellom mange flere befruktede egg enn i dag, og at forskere kan ha mer eller mindre ubegrenset tilgang til å forske på befruktede egg.
Dette er muligheter vi må forholde oss til dersom man klarer å bruke lett tilgjengelige kroppsceller fra mennesker til å lage kjønnsceller på laboratoriet.
Science fiction, tenker du kanskje – men nei. Det vil si, vi er et godt stykke unna nye tilbud på klinikkene for assistert befruktning. Før vi kommer så langt, er det mange vurderinger som må gjøres. Er det trygt? Ønsker vi dette? Hvem skal få lov?
Forskningen venter likevel ikke på at samfunnet skal ta diskusjonen, og har tatt store skritt de siste årene.
Musehaleunger
Allerede i 2012 rapporterte forskergruppen til professor Mitinori Saitou i Japan at de hadde fått frem museunger fra stamceller som de hadde stimulert til å bli eggceller. I 2016 rapporterte gruppen at de hadde fått frem musunger fra hudceller hentet fra musehaler. Musehaleungene har fått friske musunger i flere generasjoner etterpå.
Så, i 2018, ble det også klart at denne japanske forskergruppen hadde klart å lage et forstadium av menneskelige eggceller, kalt oogonium, fra en kvinnes blodceller. Her er det ikke snakk om modne egg ennå, så de kan ikke befruktes og utvikle seg til embryo.
Når det gjelder sædceller, viste kinesiske forskere i 2016 at de fikk frem friske museunger i flere generasjoner fra tidlige stadier av sædceller utviklet fra stamceller. Britiske forskere skal ha kommet et godt stykke på vei mot å lage menneskelige sædceller i laboratoriet.
Ønsker debatt

– Vi ønsker å få i gang samfunnsdebatten om temaet. Det er viktig at folk får vite hva som skjer nå. Bioteknologirådet har kommet med en uttalelse om dette som oppsummerer hvor langt fagfeltet er kommet, sier Elisabeth Gråbøl-Undersrud, seniorrådgiver i Bioteknologirådet.
«Kunstige» eller «syntetiske» kjønnsceller er blant betegnelsene som brukes. Bioteknologirådet bruker ganske enkelt begrepet «kjønnsceller laget fra andre celler». Enkelte snakker om kjønnsceller som er «avledet fra stamceller», «avledet fra hudceller» eller «avledet in vitro».
«In vitro» er latin og betyr egentlig «i glass». Innen medisin og biologi brukes begrepet for å beskrive noe som foregår i et prøveglass eller utenfor en levende organisme. Uansett hvilke navn vi gir disse cellene, er det på tide å forberede seg på en ny metodikk for unnfangelse.
IVG: in vitro gametogenese
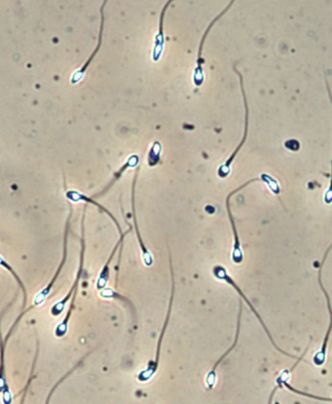
I fjor var det 40 år siden Louise Brown ble født, verdens første barn laget ved hjelp av assistert befruktning eller in vitro fertilisering (IVF). Innføringen av IVF var også kontroversiell, understreker Péter Fedorcsák, lege og avdelingsleder ved Reproduksjonsmedisinsk avdeling ved Kvinneklinikken ved Oslo universitetssykehus (OUS).
.png)

– I dag er rundt fire prosent av alle barn som fødes i Norge et resultat av prøverørsbehandling, så vi kan trygt si at dette nå har blitt godt akseptert, sier han.
Prosessen med differensiering og modning av kjønnsceller kalles gametogenese, og når dette gjøres på laboratoriet, heter det in vitro gametogenese (IVG).
Dersom forskningen kommer så langt at det blir aktuelt å tilby dette i forbindelse med assistert befruktning, mener Fedorcsák at man bør være mer varsom enn ved innføringen av IVF. Den kom nemlig før det var avklart om teknologien var trygg.
– De første årene med IVF ble svangerskapene behandlet som risikosvangerskap. Man visste ikke hva det innebar verken for mor eller barn. I dag tenker vi nok litt annerledes rundt sikkerhet, sier han.
Grunnforskning
Det er et ganske lite internasjonalt forskningsmiljø som kniver om å være først ute med å lage menneskelige eggceller og sædceller på laboratoriet. Disse forskerne er samtidig del av et hurtig voksende felt hvor målet er å forstå hvordan celler differensierer seg, og dermed også hvordan sykdom oppstår.

Selv om en av følgene kan bli muligheten for å lage babyer fra hudceller, så er det slett ikke dette som er den viktigste motivasjonen for fagfeltet som helhet, understreker
Fedorcsák.
– Forskningen på å omprogrammere celler så de får samme egenskaper som kjønnsceller, er veldig prinsipielt viktig, sier han.
Så fort et egg blir befruktet, blir det dratt i gang en symfoni av biologiske signaler som dirigerer celledeling, vekst og spesialisering, slik at et helt nytt menneske dannes. Forskerne ønsker å forstå cellenes ulike stadier, og gjerne kopiere dem i laboratoriet også.
– I dette perspektivet vil det være en helt enestående prestasjon å omprogrammere vanlige celler til kjønnsceller, sier Fedorcsák.
Han får støtte av seksjonsleder Arne Klungland ved OUS. Klungland leder en forskningsgruppe som er spesielt interessert i den genetiske reprogrammeringen som foregår når en kjønnscelle blir til. Han understreker at veldig mye av feltet handler om å forstå humane sykdommer.
– Når kroppen selv lager kjønnsceller, skjer en enorm omprogrammering hvor de rette genene blir skrudd av og på. Det er viktig å forstå denne prosessen. Å forstå hvordan en eggcelle blir til et helt individ kan for eksempel være viktig for forståelsen av hvordan en celle kan bli til en kreftcelle, sier han.
Lovverket
Uavhengig av hva som er hovedmotivasjonen for forskningsfeltet, er det ingen tvil om at biologiske grenser vil flyttes dersom forskere klarer å gjøre hudceller eller andre celler fra mennesker om til kjønnsceller.
– Ved å være tidlig ute med informasjon om hva som foregår i forskningsmiljøene, har vi en mulighet til å fremme en etisk debatt i samfunnet før disse teknologiene eventuelt blir aktuelle i klinikken, sier Gråbøl-Undersrud i Bioteknologirådet.
På et felt hvor teknologien og forskningen utvikler seg raskt, kan det være vanskelig for lovverket å henge med. Bioteknologiloven er under revisjon, og det ligger an til den første store endringen av loven siden 2005. I mars presenterte regjeringspartiene en endringsliste med 23 punkter, men ingen av disse var relatert til IVG.
– Når politikere skal gjøre endringer i lovverket, er det viktig at de har kjennskap til hvordan nye teknologier fundamentalt kan endre hvordan reproduksjon foregår, sier Gråbøl-Undersrud.
Trygt?
Klungland understreker at det ikke er sikkert at det noen gang blir aktuelt å vurdere IVG i forbindelse med assistert befruktning. Dersom teknologien til slutt blir vurdert som trygg, tror han det kan ta alt fra 10 til 30 år før vi ser den i klinikkene.
– Men om du hadde snakket med meg for ett år siden, hadde jeg sikkert sagt at det er 10-20 år til vi får se den første genredigerte babyen også, legger han til.
Det ble stor oppstandelse i november 2018, da det ble kjent at verdens første genredigerte babyer var født. En kinesisk forsker sto bak, og verden reagerte med sjokk og vantro. Det er bred enighet om at det foreløpig ikke er forsvarlig å lage slike arvelige genetiske endringer.
Også på veien mot å ta i bruk IVG til assistert befruktning, er første punkt å avgjøre om teknologien er trygg.
– Selv om dette fungerer hos mus, er det ingen garanti for at det vil fungere hos mennesker, sier Klungland.
På den andre siden: dersom gjennombruddet blir et faktum, er det ikke uoverkommelig å dokumentere at teknologien er trygg nok til å faktisk prøve ut på mennesker.
– Dette må prøves ut i dyremodeller først. Deretter må humane kjønnsceller laget i laboratoriet testes veldig nøye opp mot sædceller og eggceller som er produsert i kroppen, forklarer Klungland.
Med andre ord må forskerne sjekke om omprogrammeringen de har gjort i laboratoriet er akkurat den samme omprogrammeringen som kroppen selv gjør når den lager kjønnsceller.
– Det er fullt mulig å sjekke dette, men den endelige bekreftelsen på om dette er trygt, vil vi ikke få før noen lager et menneske på denne måten, sier Klungland.
Biologiske grenser
Selv om teknologien skulle vise seg å være trygg, er det ikke sikkert at samfunnet aksepterer den.
– Et av de mest utfordrende aspektene ved IVG er at teknologien løser opp biologiske grenser, sier Anna Smajdor, førsteamanuensis i filosofi ved Universitetet i Oslo.
Hun skrev doktorgraden sin om temaet, og mener det er svært viktig å tenke gjennom utfordringene som kan være knyttet til en slik teknologi på forhånd.
Så hva bør vi tenke gjennom? En av de biologiske grensene som kan gå i oppløsning, er kvinners overgangsalder. Det er knapp tilgang på eggceller i dag, og kvinnekroppen lager dem kun frem til menopausen.
– Med IVG vil ikke kvinnenes alder bety så mye, siden det er fullt mulig å bære frem barn etter overgangsalderen, så lenge kvinnene har tilgang på egg, sier Smajdor.
Menn har alltid kunnet bli fedre frem til de er langt opp i åra. IVG vil kunne utjevne denne kjønnsforskjellen, men vil det være bra for barna?
Alle kan bli foreldre
Det vil også være teoretisk mulig å lage egg- eller sædceller fra hudcellene til en nyfødt. Tenk deg et foreldrepar som er i ferd med å miste et barn. Skal de kunne lage kjønnsceller for dette barnet og deretter bære fram sitt eget barnebarn?
Om teknologien fungerer, vil det også være biologisk mulig å bruke celler fra en kvinne til å lage sædceller, og celler fra en mann til å lage egg. På den måten vil par av samme kjønn kunne få barn som er genetisk beslektet med begge.
Alle disse mulighetene reiser nye spørsmål rundt hvem som skal ha tilgang til assistert befruktning.
Da man startet med IVF gikk helsevesenet langt for å ivareta sæddonors anonymitet. I 2005 ble reglene for sæddonasjon endret med åpning for at barnet kan få vite navnet på donor fra det fyller 18 år. Nå vil regjeringspartiene innføre en plikt for foreldre til å informere barnet dersom det er unnfanget gjennom assistert befruktning, for å ivareta barnets rett til å kjenne sitt biologiske opphav.
– Utviklingen forteller en del om hvordan våre holdninger til ny teknologi kan endre seg, sier Klungland.
Moralsk status
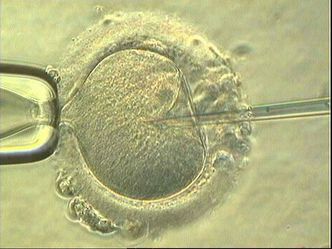
I dag må kvinner gjennom en ganske tøff behandling i forbindelse med IVF. Den involverer både hormonbehandling og kirurgi. Bare et begrenset antall egg kan hentes ut. Hva blir konsekvensene dersom det blir mulig å bruke hudceller til å lage mange flere egg, kanskje hundrevis eller tusenvis, for hver kvinne?
Gråbøl-Undersrud i Bioteknologirådet tror en slik utvikling vil kunne gjøre det mer aktuelt å velge ut embryo med ønskede gener.
– Her nærmer vi oss debatten om sorteringssamfunnet og designbabyer igjen, sier hun.
Tilgangen på eggceller har vært en viktig begrensning for forskningen på befruktede egg også. I Norge har det kun vært lov til å forske på befruktede egg som er til overs ved IVF-behandling. Vil dette forandre seg dersom forskere kan bruke IVG til å skaffe slike celler?

– I dag er det veldig streng regulering på å studere humane egg, sædceller og befruktede egg. Jeg mener det er viktig at reguleringen er like streng dersom man skal bruke IVG, sier Klungland.
Smajdor understreker på sin side at all eksisterende regulering av bruken av embryo i forskning er basert på ideen om at eggceller er vanskelig å få tak i. Dersom cellene kan lages på laboratoriet, utfordrer det rammene for denne forskningen.
– Vi risikerer at embryo og kjønnsceller mister den spesielle moralske statusen de har i dag. Er vi villige til å la dette skje? Det er et viktig etisk spørsmål, sier hun.