Kongsberg Beam Technology er navnet gründer Per Håvard Kleven har gitt selskapet. Kleven er en kjent mann på Kongsberg. Han jobbet over 20 år i kongsbergindustrien, før han etablerte Devotek, som han etter 14 år solgte til Semcon i 2015. Det var da han begynte å jobbe for fullt med ideen han allerede hadde tenkt på noen år, og som han nå håper skal kunne revolusjonere strålebehandlingen. Foreløpig har han ikke en gang en fungerende prototyp, men med patenter i boks og en rekke sterke samarbeidspartnere med tro på teknologien, er målet å være klare for markedet fra 2024.
– Vi vil kombinere den mest avanserte formen for strålebehandling med de mest avanserte styringssystemene fra industrien. Det er først nå alle byggeklossene vi trenger innen kunstig intelligens, digitale tvillinger og maskinlæring er på plass. Nå er tiden inne for å realisere ideen, sier Kleven.
Bedre kontroll
I dag behandles de fleste kreftpasienter i Norge med fotoner, ved at lineærakseleratorer retter høyenergetisk røntgenstråling så presist som mulig mot svulsten. Slik stråling har høy gjennomtrengingsevne, men bestråler samtidig friskt vev både foran og bak svulsten i hele strålebanen gjennom kroppen. Dermed står man i fare for å ikke bare drepe kreftcellene, men også friske celler. Det kan gi alvorlige bivirkninger og senskader for pasienten.
Derfor anses protonstråling som mindre risikofylt. Protoner er relativt tunge, ladede kjernepartikler som akselereres i en syklotron til to tredjedeler av lysets hastighet før de siktes mot pasienten. Protoner dreper kreftcellene på samme måte som fotoner, men skader ikke normalvevet rundt svulsten like mye som konvensjonell stråling, fordi de går rettlinjet i vevet med en mer presist definert rekkevidde avhengig av tilført energi, og avsetter denne energien i et begrenset område der de stanser.
I praksis betyr det at man i større grad kan styre hvor energien «slippes løs» slik at behandlingen blir mer presis, og at en svært liten dose avsettes i omliggende normalvev. Dette kan føre til at flere pasienter blir friske, og med færre bivirkninger enn ved fotonbehandling.
Kongsberg Beam Technology mener imidlertid at de skal kunne ta protonbehandlingen til et nytt nivå.
Presisjon og prediksjon
Systemet de har patentert heter MaMa-K, en forkortelse for Multi-Array Multi-Axis Cancer Combat Machine.
Inspirert av systemer for hiv-kompensasjon offshore, skal systemet kompensere for det faktum at svulsten beveger seg selv om pasienten ligger fiksert på behandlingsbordet.


– I dag velger man en energi på partiklene med bakgrunn i en «frossen» utgave av pasienten: Du ser hvor tumoren var i bildene av pasienten du benyttet da du laget behandlingsplanen, og sveiper over pasienten med en energi på partiklene som er tilstrekkelig til å nå akkurat det dypet. Men om du skal behandle kreft i buken, bekkenet eller lungene er det organer som flytter på seg hele tiden, samtidig som pasienten selvfølgelig puster og hjertet slår. Dermed er ikke tumoren fiksert selv om pasienten er det, og tettheten kan ha forandret seg slik at rekkevidden på partiklene forandres. Dagens teknologi gjør det ikke mulig å justere behandlingen etter slike kriterier, forklarer seksjonsleder Karsten Rydén-Eilertsen ved Avdeling for medisinsk fysikk ved Oslo universitetssykehus Radiumhospitalet.
Han utførte den kliniske delen av mulighetsstudiet for Kongsberg Beam Technology i fjor.
For å kompensere for slike usikkerhetsmomenter lager man gjerne partikler med litt for høy energi for å være sikker på å nå helt inn til tumor, men om tettheten har blitt mindre siden behandlingsplanen ble laget, risikerer man at partiklene for eksempel går forbi tumor og inn i et risiko-organ som hjerte eller lunge før de avsetter energien sin. Det er naturlig nok ikke ønskelig.

– Hvis du ikke kan ta høyde for disse faktorene, må du legge inn så mange sikkerhetsmarginer i behandlingen at du ikke får utnyttet protonenes store fordel med at de avsetter energien sin på slutten av partikkelsporet fullt ut. Om man kan følge endringer i kroppen, slik at man har kontroll på akkurat hvor partiklene går, vil det være en stor fordel, sier Rydén-Eilertsen.
Denne kontrollen mener Kongsberg Beam Technology de skal få ved å lage en dynamisk digital tvilling av pasienten, som ved hjelp av kunstig intelligens, maskinlæring og prediksjon vil gjøre det mulig for behandlingsplanen å oppdatere seg selv i sanntid mens pasienten ligger på behandlingsbordet.
– Når programvaren er opplært til å tolke hvordan ting typisk beveger seg i menneskekroppen, og lærer ulike mønstre hos ulike pasienter, har vi et godt utgangspunkt. Når vi da samtidig skanner pasienten med røntgen eller CT under behandlingen, vil det gjøre at modellen kan forutse bevegelser og gi nok prediksjon til at protonstrålenes retning og styrke kan følge svulsten med millimeterpresisjon, sier Per Håvard Kleven.
.png)

Selve produktet
Men dagens protonstråleanlegg er ikke utviklet for å kunne endre retning, innfallsvinkel og styrke på energien i sanntid. Mens den digitale tvillingen i hovedsak kan ferdigstilles med systemutvikling, programmering og kjøp av hyllevareløsninger, er det her Kongsberg Beam Technology virkelig har måttet tenke helt nytt med MaMa-K.

– Vi har utviklet og patentert en løsning for en helt ny kanon som kan kobles til alle eksisterende protonanlegg og erstatte stråledysen de har i dag. Det er den som er selve produktet vårt, sier Kleven. Kanonen heter Particle Beam Guiding Tube.
Karsten Rydén-Eilertsen forklarer at en standard protonmaskin i dag har en stor tut (nozzle) som retter protonene mot pasienten og kan sveipe ut fra dette fikserte punktet med en pennestråle, litt på samme måte som katodestrålerørene fungerte i gamle svart/hvitt-tv-er. Dette er dagens strålekanon der nozzelen er montert på et såkalt gantry, som i prinsippet er en veldig stor sirkelformet kranmodul som går 360 grader rundt pasienten. Om strålen skal vinkles i et nytt sveipemønster, må gantryet roteres. Det tar relativt lang tid – cirka en halv time – å rotere én runde rundt pasienten.
– Particle Beam Guiding Tube vil være mye mer dynamisk enn det. Den vil ha flere stråleutgangspunkt samtidig, og endre sveipemønsteret mye mer fleksibelt og raskere enn det du kan med dagens standardmaskiner, sier Rydén-Eilertsen.
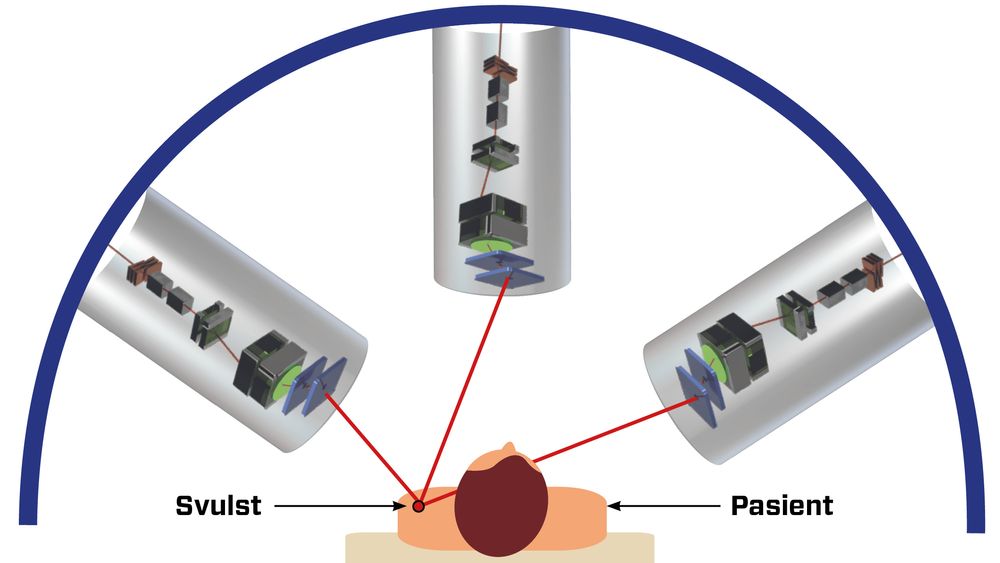
Den største effekten i så måte får de fordi deres nye produkt er tenkt levert med tre kanoner, slik at svulsten til enhver tid kan bestråles i tre akser. Data fra den digitale tvillingen og den sanntidsoppdaterte behandlingsplanen vil bestemme hvilken kanon som stråler i hvilken styrke, og skal også kunne koble ut en eller to av kanonene dersom de har feil vinkel eller dybde i forhold til risiko-organer eller lignende. Protonene skal styres av superledende magneter, slik at kryogen kjøling må bygges inn i kanonene. I tillegg fylles de opp med elektronikk, sensorer og programvare.
Kongsberg Beam Technology AS
- Gründerselskap som utvikler et system kalt MaMa-K som ved å kombinere avanserte styringssystemer med en mer presis strålekanon skal gjøre protonstråling av kreftsvulster mer presist, billigere og med færre bivirkninger enn dagens behandlingsalternativer.
- Startet med konseptutvikling og patentsøknader i 2016. Mulighetsstudie i 2018, både klinisk og systemteknisk, viste at løsningen er gjennomførbar og vil gi nytteeffekter.
- Ledes og eies (97%) av gründer Per Håvard Kleven. En CEO er ansatt, men navnet er ennå ikke offentliggjort. Kongsberg Innovasjon, Oslo Cancer Cluster Incubator og Vestlandets Innovasjonsselskap er inne på eiersiden med 1% hver.
- Partnere: Avdeling for medisinsk fysikk ved Oslo Universitetssykehus / Radiumhospitalet, Semcon Norge, Avdeling for radiologi-nukleærmedisin ved Universitetet i Oslo, OncoRay (Tyskland), Onsagers AS.
- Har fått økonomisk støtte fra Innovasjon Norge, Skattefunn, Oslofjordfondet og Buskerud fylkeskommune gjennom Forskningsrådets Forregion-program.
– Miljøet inne i selve kanonen er veldig komplekst, men vi skal lage styringssystemer for noe som står stabilt og stille i et veldig kontrollert miljø uten fiender som skyter på det. Det gjør utviklingen mye billigere enn for mye annet som utvikles på Kongsberg, sier Per Håvard Kleven.
Trenger 30 millioner
Billig er det likevel ikke. Totalt vil de trenge 95 millioner kroner de neste årene for å ha et produkt klart i 2024. I første omgang er de på jakt etter 15 millioner kroner fra private investorer, og tilsvarende fra virkemiddelapparatet – i tillegg til de 8 millionene de fikk fra Skattefunn i mars i år. Det skal bringe dem to år fremover.
– Nå har vi noen år foran oss med utvikling av de forskjellige delene av systemet før vi kommer til fullskalatesting og kvalifisering. Vi begynner med å bygge opp magnetsystemer som gjør oss sikre på at vi klarer å styre strålen så presist som vi ønsker, og å utvikle et system som er selvlærende slik at strålen følger svulsten når den beveger seg, sier Kleven.
– Hva er den største teknologiske utfordringen?
– Det er å klare å styre strålen sikkert i fem akser – både X og Y hvor den kommer fra, og X, Y og Z som den skal til – med stor nok endringshastighet til å kompensere for hjerteslag og med høy nok hastighet. Den skal skifte veldig raskt, og det er ekstreme magnetfelt som må til, sier Kleven.
Direktør Bjørn Klem i Oslo Cancer Cluster Incubator følger spent med på Kongsberg Beam Technology:
– Jeg tenker det må være glimrende om man får et system til å fungere som ikke minst kan åpne opp for at nye pasientgrupper kan få protonbehandling fordi man reduserer bivirkningene og risikoen så mye. For oss er det i tillegg ekstra morsomt å kunne bidra i et prosjekt som vil kunne stå for mye interessant forskning i det nye protonsenteret som nå bygges ved Radiumhospitalet, sier han.
Protonbehandling
Stadig flere pasienter overlever kreft, men langtidsbivirkninger er et økende problem fordi intens medikamentell behandling og stråling blir brukt i behandlingen. Målet med protonbehandling er at flere skal overleve og leve lengre med færre langtidsskader etter kreftbehandling.
Behandling med protoner som alternativ til ordinær strålebehandling med fotoner gjør det mulig å gi høyere stråledoser til dyptliggende svulstvev og tilsvarende lavere doser til nærliggende normalvev – med mindre skader på vevet.
Basert på dagens kunnskap regner man med at 10-15 prosent av pasientene som henvises til strålebehandling vil ha bedre nytte av protonterapi. Særlig barn anbefales protonterapi for å få mindre senskader. I dag sendes mellom 50 og 100 norske barn til utlandet for protonbehandling hvert år. Hver slik behandling koster cirka 1 million kroner.
Stortinget vedtok i statsbudsjettet for 2018 at det skal etableres to protonsentre i Norge. Senteret i Oslo får to behandlingsrom og et forskningsrom og skal åpne ved Radiumhospitalet i 2023, og senteret i Bergen får et behandlingsrom og et forskningsrom, og skal åpne ved Haukeland universitetssykehus i 2024. Kostnadsrammen på de to sentrene totalt er 3,1 milliarder kroner.
2. mai fikk Varian Medical Systems kontrakten som leverandør av utstyr til protonterapi både i Oslo og Bergen. 23. mai startet riving og klargjøring av tomten slik at byggingen av protonsenteret på Radiumhospitalet kan starte.