En leser av Ingeniøren, Anne Grete Rasmussen, har spurt:
Flere tyske uavhengige og kompetente kilder beskriver at uløselig kaliumsitrat dannes hvis sitronsyre brukes til avkalking ved høye temperaturer på f.eks. kaffemaskiner og vaskemaskiner.
Som rengjøringsekspert anbefaler jeg derfor bare å bruke sitronsyre i lunkent vann. Men jeg har ingen vitenskapelige bevis for at avkalking med sitronsyre er effektivt med lunkent vann, og om det stemmer at det dannes uoppløselige belegg med kaliumsitrat.
Imidlertid har jeg sett vaskemaskiner med belegg som ikke kunne fjernes.
Sitron- eller eddiksyre?
Den samme leseren vil også gjerne vite:
Hvordan er aggressiviteten til sitronsyre eller eddiksyre mot materialene som finnes i en vaskemaskin?
Tidligere ble det anbefalt bruk av sitronsyre i vaskemaskiner av vaskemiddelprodusenter. Nå selger de dyre pakker med sitronsyre. Hvorfor ikke bruke den mye billigere eddiksyren?
Problemet med mye kalk i vaskemaskinene har vokst etter at fosfater ikke lenger var tillatt å bruke i vaskemidler, og ikke minst etter at EU endret skalaen for vannhardhet.
Litt om syrer
Anton A. A. Smith, forsker i kjemi ved DTU, svarer:


Dette handler om kalsiumsitrat, ikke kaliumsitrat.
Årsaken må finnes i den molekylære strukturen til sitronsyre.
Først litt om syrer: Det er forskjellige definisjoner av hva en syre og en base er i kjemi, men for å svare på dette spørsmålet sier vi at en syre er et stoff som kan avgi et proton, den positivt ladede ioniske formen av hydrogen, og en base kan ta opp et proton (H +).
Kalk er et salt som består av kalsiumkarbonat, CaCO3, hvor de respektive ionene i saltet er Ca2+ og CO32- (karbonat). Dette har en utrolig lav løselighet, og når syre tilsettes, kan karbonat-ionen, CO32-, reagere som en base og motta protoner, H+, og karbondioksid, H2CO3, dannes.
Det er den samme syren som dannes når CO2 og vann blandes, og denne reaksjonen er en likevekt og kan gå begge veier. Så når karbondioksid dannes ved å blande en syre og kalk, dannes karbondioksid, som deretter spontant omdannes til vann og CO2. Derfor bobler det når du avkalker.
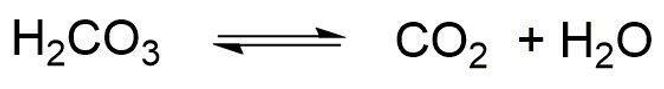
Negative ladninger har en effekt på dannelsen av salter
Det som er igjen er et salt som består av syreresten fra syren som brukes, samt kalsium-ionen. Hvis du bruker eddiksyre, dannes kalsiumacetat, og hvis du bruker sitronsyre, dannes kalsiumsitrat osv.

%2520propulsion%2520pic%25206.jpg)
Sitronsyre har tre syregrupper som kan frigjøre protoner, og når de frigjør disse positivt ladede protonene, har den deprotonerte sitronsyren (såkalt sitrat) tre negative ladninger. Dette er viktig ettersom antallet negative ladninger på et molekyl har stor innvirkning på hvordan det danner salter, for eksempel kalsiumsitrat.
Kalsium-ioner har to positive ladninger, så når kalsium og sitrat danner salter, skjer det i et forhold mellom to sitratmolekyler og tre kalsium-molekyler, slik at den totale ladningen for saltet er 0. Bindinger basert på hele elektriske ladninger kalt ioniske bindinger.
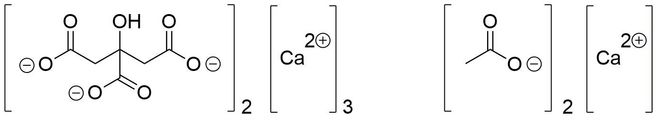
I kalsiumsitrat er det mange ladninger som er tett pakket sammen, og mange vannmolekyler er nødvendige for å holde dem atskilt. Løseligheten ved 25 ° C er ca. 0,95 g / L. Omvendt er kalsiumacetat mer vannløselig, da eddiksyreresten (acetat) bare har en enkelt negativ ladning.
Saltet dannes i et forhold på 2 x acetat per kalsiumion. Det er lettere for vann å skrelle fra hverandre, og løseligheten er ca. 300 ganger større enn for kalsiumsitrat.
Kanskje større risiko for salter ved høye temperaturer
Der det bryter litt med intuisjonen er med temperaturen. Oftest øker løseligheten til salter med temperaturen, men dette er ikke alltid tilfelle, og det er det ikke med kalsiumsitrat.
En nylig studie fra Københavns universitet har vist at vann danner to forskjellige kalsiumsitratsalter som inneholder forskjellige mengder vann i krystallstrukturen, et salt med fire (kalsiumsitrat tetrahydrat) og ett med seks (kalsiumsitrat heksahydrat).
Tetrahydrat-saltet dannes fortrinnsvis ved høyere temperaturer og har i tillegg lavere vannløselighet ved høyere temperaturer enn ved lavere temperaturer.
Så veldig kort: Det er større risiko for dannelse av kalsiumsitratsalter ved avkalking ved høye temperaturer enn ved romtemperatur, men hvis du ser på dataene i studien ovenfor, er det ikke stor forskjell.
Imidlertid er rådene dine om bruk av lunken sitronsyre ganske gode, da det burde være i stand til å håndtere oppgaven uten problemer. Hvis det er mye kalk, kan det muligens tas over 2-3 runder, hvis løsningen skulle bli mettet med kalsiumsitrat.
Eddiksyre vs. sitronsyre
Til slutt skal det nevnes at kalsiumsitrat ikke er uoppløselig i vann, og hvis det dannes, kan det oppløses, selv om noe vann er nødvendig.
Når det gjelder spørsmålet om eddiksyre vs. sitronsyre: Begge takler oppgaven uten problemer.
Hvis materialene er laget for å feste sitronsyre, håndterer de også eddiksyre. Eddiksyren bør imidlertid ikke konsentreres, da den i seg selv er et organisk løsningsmiddel og kan skade gummimembraner ved å fungere som en mykner av plast.
Denne artikkelen ble først publisert på Ingeniøren.




