Over hele verden står svært syke mennesker i kø for å få nye organer transplantert. I Norge dreier seg om rundt 400 personer, og i USA så mange som 100.000. I Norge dør rundt 20 av de som står i kø hvert år uten å ha fått hjelp, mens i USA dør et tilsvarende antall daglig.
Å bruke organer fra dyr har vært prøvd før, uten særlig hell. Det er flere dyr som har ganske lik størrelse og form på organer som potensielt kunne ha passet mennesker, hvis det ikke var for immunsystemets aggressive angrep på alt som ikke gjenkjennes som kroppens eget.
Det er akkurat det samme man opplever når man transplanter organer mellom mennesker, men her er overflatemolekylene på cellene like nok til at man kan hindre avstøtning ved å påvirke immunsystemet med dempende medisiner. Skal man transplantere mellom arter er utfordringene mye større, fordi ulikheten i overflatemolekylene er så stor. De virker som markører som trigger immunsystemet til å angripe.
- Israelske forskere: Hevder de har 3D-printet et hjerte
Fjerne innebygde virus
Et annet potensielt problem er at DNA fra en art kan inneholde rester av virus som har blitt til en del av artens DNA. Faktisk stammer så mye som 8 prosent av menneskets DNA fra virus, men disse virusgenene gjør normalt ingen skade. Får vi celler eller organer fra en annen art kan slike innebygde virusgener derimot potensielt være et problem. Det ønsker vi ikke å ta sjansen på.
Med Crispr-teknologi er det er mulig å løse dette. Denne teknologien gjør det mulig å utføre helt presise kutt i DNAet. Med den metoden har forskere klart å skape en gris helt uten de 62 såkalte PERV-virusgenene som normalt ligger i grisens DNA. Grisen har en litt kortere DNA-streng, men skiller seg ikke ellers fra andre griser. Dermed er man kvitt bekymringen for om virusene kan utløse sykdom hos pasienten.
På samme måte som man har klart å fjerne virus fra DNA, jobbes det med å endre eller fjerne overflatemolekyler fra dyrecellene som gir avstøtningsreaksjoner. Utfordringen er å kunne fjerne eller modifisere nok, uten at det går ut over cellenes levedyktighet.
Flere oppstartselskaper jobber med dette, og målet er å lage dyreorganer som ikke gir avstøtningsreaksjoner i mennesker. Får de til det, blir ikke resultatet begrenset til ett organ. Hele dyret blir i så fall mer biokompatibelt med mennesker.
Om dette gir tilstrekkelig biokompatibilitet er mange skeptiske til. De mener man fortsatt kan få for kraftige avstøtningsreaksjoner til at slike organer kan benyttes til transplantasjoner.
- Stamcelleforsker: Tror organproduksjon er rutine innen ti år


Dyrke sine egne organer
En annen vei å gå er å bruke et dyr, en gris eller en sau, til å dyrke fram et helt nytt organ basert på cellene til den som trenger organet.
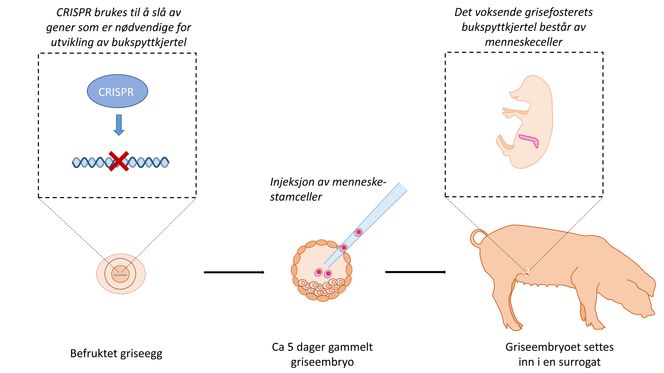
For eksempel kan diabetikere ha behov for ny bukspyttkjertel som kan produsere insulin. Med Crispr-teknologi kan man klippe ut eller slå av de genene som koder for bukspyttkjertelen i f.eks. et griseembryo. Et slikt embryo vil i så fall utvikle seg til en gris uten bukspyttkjertel.
I dag er det mulig å lage stamceller fra hudceller. Slike celler kan brukes til å bygge alt mulig av vev gitt de riktige betingelsene. Ved å sprøyte stamceller fra pasienten inn i embryoet lages en menneskelig bukspyttkjertel i tomrommet der grisens bukspyttkjertel skulle vært.
Forskere i USA har vist at dette er mulig. Andelen menneskeceller i griseembryoene var imidlertid for lav til at en transplantasjon ville vært vellykket, fordi det ville fulgt med for mange griseceller.
I forsøk med bruk av saueembryo ble resultatet mer «menneskelig», og derfor mer vellykket.
Selv om disse forsøkene viser at det kan være teknologisk mulig å dyrke menneskeorganer i dyr, har de så langt blitt stoppet etter noen uker, lenge før dyrene ble født, av etiske årsaker.
Det gjenstår derfor å se om slike organer blir genetisk like nok til at man kan unngå alvorlige avstøtningsreaksjoner. Men i forsøk mellom rotter og mus, der den samme teknikken ble brukt for å gi musen en bukspyttkjertel dyrket fra sine egne celler i en rotte, fungerte transplantasjonen uten avstøtning, og kurerte musens diabetes.
.png)

- Bioprinting av vev og organer: Vil presse fram etisk debatt
Mange dilemmaer
Selv om det utvikles teknologi som kan gi oss tilstrekkelig med tranplanterbare organer, er det mange praktiske og etiske utfordringer knyttet til feltet.
For det første trengs det dyr som har organer som på alle måter er mest mulig lik de menneskelige, blant annet i størrelse og form.
Det er også en utfordring knyttet til stamceller. Når man lager stamceller fra huden til f. eks. en 60-åring, vil cellene i organet bære preg av at de er gamle. Blant annet er man bekymret for at de kan bli kreftceller.
Og når man lager en gris som har menneskeceller, hva har man laget da? Kan vi spise resten av grisen når vi har hentet ut organet den ble født for å lage - den er jo dels menneskelig?
Om en behandling som dette blir mulig, er det etisk uforsvarlig å gjennomføre behandlingen, eller veier det etisk tyngre å redde livet til et menneske?
- Genetisk forskning: Skal få bakterier til å fungere som organer
Forbudt
Under gjeldende regelverk er uansett en slik transplantasjon forbudt i mange land, også i Norge. Men den raske teknologiske utviklingen har fornyet debatten, og i USA vurderer myndighetene om de skal endre loven slik at denne typen forskning og behandling kan tillates. Det står allerede et selskap klart til å søke om tillatelse til å prøve transplantasjon med sine Crispr-redigerte griseorganer.
CRISPR
- En forkortelse for Clustered Regularly Interspaced Short Palindromic Repeats. Dette er en teknologi som er hentet fra det primitive immunsystemet som bakterier har utviklet for å forsvare seg mot virus.
- Her utnyttes et protein (Cas) som binder seg til DNA og bestemmer akkurat hvor et kutt skal gjøres. Når DNA-strengen er kuttet vil cellen reparere den.
- CRISPR er en svært mye mer presis måte å flytte gener inn og ut i DNA enn den vi har benyttet siden 80-tallet.
- Teknologien er også enkel i bruk og kan gjøre flere varianter av endringer enn tidligere metoder. Det har gjort at anvendelsen har skutt fart, og gitt resultater vi knapt kunne drømme om for ti år siden.
Det er imidlertid ikke sikkert at vi trenger xenotransplantasjon for å løse problemet med organmangel.
Det utvikles også andre teknologier, for eksempel basert på såkalt bioprinting der organer bygges opp av biokompatible materialer i en 3D-printer som injiseres med stamceller. Man tror at slik teknologi i hvert fall skal kunne brukes til å fremstille organer med enkle strukturer som nyrer og blærer, men at det på lengre sikt skal kunne brukes til mye mer komplekse organer. Israelske forskere hevder allerede at de har klart å 3D-printe et hjerte.
Det er mye som tyder på at all denne teknologien kommer til å bli brukt. Spesielt store land som Kina og USA vil nok gjøre et forsøk og utvikle feltet. De trenger både mye organer, og kjemper om ledertrøya innen bioteknologi.
Kilde: Seniorrådgiver i Bioteknologirådet, Sigrid Bratlie
- Kan erstatte transplantasjon: Norsk kirurg lager kjevebein fra-stamceller



