Ved Universitetet i Oslo jobber flere forskere med å lage nye stoffer som de håper vil egne seg som medisiner mot ulike sykdommer som kreft, astma, tuberkulose, Alzheimers og Parkinsons. De må teste mange stoffer før de finner noe som kan brukes.
Å lage en ny medisin tar vanligvis ti til tjue år. Et viktig trinn på veien er å finne ut hvordan man skal framstille virkestoffene i medisinen i laboratoriet.
Både professor Lise-Lotte Gundersen ved Kjemisk institutt og professor Trond Vidar Hansen ved Farmasøytisk institutt ved Universitetet i Oslo (UiO) jobber med denne innledende fasen av utviklingen av en ny medisin.
Les også: Vil erstatte dyreforsøk med datasimulering
Lang vei til målet
Bare en brøkdel av stoffene som lages og testes, ender opp som medisiner.
Gundersen har for eksempel allerede testet ca. 600 stoffer som likner på hverandre, på tuberkulosebakterier.
– Av 20 000 molekyler som testes i rotter, mus og hunder, vil kun ti molekyler bli testet i mennesker. Av disse ti vil normalt ett nytt legemiddel bli resultatet, forteller Hansen.
Han påpeker at tallene kan varierer for ulike sykdommene og ulike typer legemidler. De avhenger også av når analysene er foretatt fordi kravene til dokumentasjon endrer seg og ny teknologi kommer til.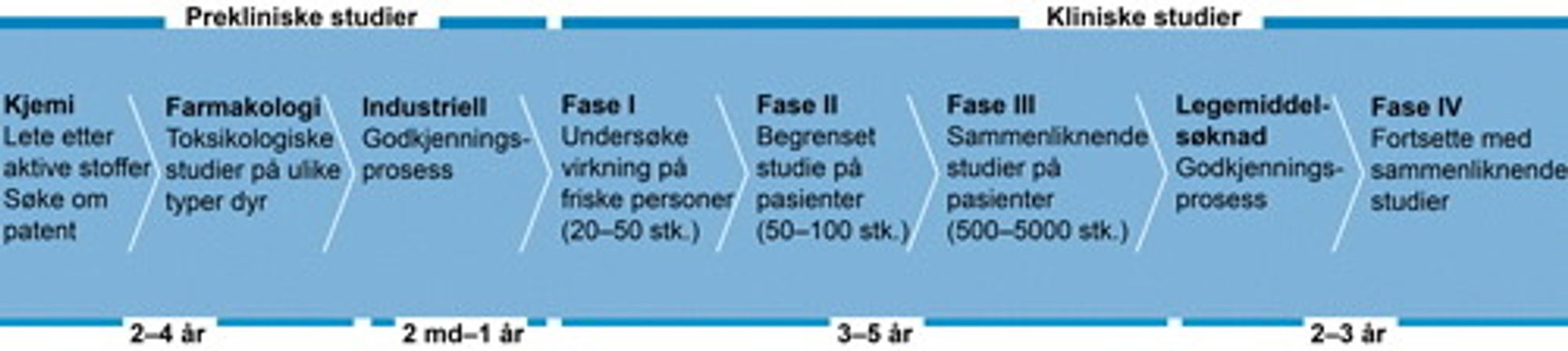
Ulike innfallsvinkler
Hvordan bestemmer så forskerne hvilke stoffer de skal lage og hvilke sykdommer de skal teste dem på?


– I ett av prosjektene jobber vi med å lage stoffer som inneholder ringstrukturer som kalles puriner, som vi håper skal kunne brukes som legemidler mot tuberkulose, forteller Gundersen.
– Det er litt tilfeldig at vi begynte å jobbe med tuberkulose. Vi hadde egentlig tenkt å undersøke om disse stoffene kunne ha noen effekt mot hiv/aids og kreft, men så fikk vi tilbud om å være med på et screeningprosjekt. Der fikk vi helt uventet flere treff på tuberkulose, så da jobbet vi isteden videre med det.
På verdensbasis dør årlig rundt to millioner mennesker av tuberkulose. Problemet med de medisinene som brukes mot sykdommen i dag, er at bakteriene er blitt resistente mot dem.
Den typen stoffer Gundersen jobber med, virker på en annen måte enn dagens medisiner, derfor mener hun at bakteriene vil bruke lang tid på å utvikle resistens mot dem.
I et annet prosjekt jobber Gundersen med såkalte adenosinantagonister, det vil si stoffer som motvirker effekten av adenosin.
– Adenosin er et signalstoff som binder til adenosinreseptorer på cellene våre og setter i gang en rekke reaksjoner. Parkinsons sykdom, astma og kreft er eksempler på sykdommer der adenosin spiller en rolle, sier Gundersen.
– Adenosinantagonister hermer etter adenosin. De binder seg til adenosinreseptorene uten selv å sette i gang noen reaksjoner. De demper dermed signalene og effekten av adenosin.
Les også: Nanopartikler i fisk kan gi kur mot tuberkulose
Lager flere liknende stoffer
Koffein som finnes i blant annet kaffe, te og sjokolade, og teofyllin som finnes i te, er eksempler på adenosinantagonister. Kjemikerne ved UiO begynte å interessere seg for adenosinantagonister etter at andre kjemikere hadde fått gode resultater med stoffer som liknet på de stoffene de jobbet med i tuberkuloseprosjektet.
Gundersen og hennes kolleger lager flere varianter av stoffene de har sett virker, for å prøve å finne stoffer som virker enda bedre enn de stoffene de allerede har.
– For adenosin vet vi mye om virkningsmekanismen til stoffene og kan modellere og tenke oss hvordan stoffene kan endres for at de skal fungere bedre. For tuberkulose derimot vet vi ikke sikkert hva som gjør at stoffene virker. Der må vi prøve oss fram og sette sammen et puslespill basert på mange testresultater, forklarer Gundersen.
Tester utenlands
Ved Kjemisk institutt lager de stoffene og bestemmer strukturen på dem. De må vise at stoffene er rene og at de kjemiske reaksjonene har gitt dem det de prøvde å lage.
Gundersen forteller at de jobber en del med metodeutvikling og å tilpasse metodene til akkurat de stoffene de skal framstille. Når de skal finne strukturen til stoffene, bruker de ulike spektroskopiske metoder, spesielt kjernemagnetisk resonans (NMR, fra engelsk nuclear magnetic resonance) og massespektrometri (MS).
Selve testingen av stoffene foregår i andre land.
– For tuberkulose sender vi stoffene til for eksempel USA der de tester dem på tuberkulosebakterier. De tester også på andre bakterier for å se om stoffene virker spesifikt mot tuberkulose, sier Gundersen.
– For adenosin er reseptoren kjent og vi tester hvordan den binder til stoffene vi har laget. Dette gjøres i Tyskland. En postdoktor herfra har deltatt i noe av det arbeidet.
Les også: Her ligger fremtidens antibiotika
Stoffer fra naturen
Gundersen prøver også å framstille såkalte asmariner i laboratoriet.
Asmariner er stoffer som produseres i marine organismer. De er funnet av andre som har screenet ekstrakt fra disse organismene i jakten på stoffer som kan egne seg som legemiddel.
Forskerne ser for seg at asmariner kan brukes mot kreft og som antibiotika. Men for å få store nok mengder av stoffene til å gjøre større forsøk, må de ifølge Gundersen framstille dem syntetisk i laboratoriet.
I laboratoriet kan de dessuten lage stoffer som likner, det de kaller analoger, som kan være lettere å lage og som kan virke bedre.
Også Hansen på Farmasøytisk institutt jobber med stoffer vi finner i naturen, nærmere bestemt sunne, flerumetta omega-3-fettsyrer som finnes i blant annet feit fisk. Han forteller at bruken av disse fettsyrene har lange historiske røtter her i landet.
– Selv vikingene kjente til omega-3-fettsyrene. De brukte dem til lampeolje, de visste at umetta fettsyrer er flytende, mens metta fettsyrer er faste, forteller Hansen.
– I 1854 utviklet farmasøyt Peter Möller en metode for å ekstrahere og destillere estere fra torskelever for å lage tran – Möller's Tran – som er rik på omega-3-fettsyrer. Han patenterte metoden som fortsatt er basis for dagens teknologi.
Les også: Snart kan du få sprøytestikk uten smerter
Tester på dyr og mennesker
Forskerne jobber nå med å vise hvorfor det er sunt å spise omega-3-fettsyrer. De bruker også fettsyrene til å lage stoffer som de håper vil egne seg som legemidler.
– I fisk og fiskeoljeprodukter som tran finner vi omega-3-fettsyrene eikosapentaensyre (EPA) og dokosaheksaensyre (DHA). I kroppen omsettes disse til metabolitter, forteller Hansen.
– I løpet av de siste ti årene har forskere vist at disse metabolittene har gunstig effekt på inflammasjoner, altså betennelser. Det er vist at inflammasjon ikke er en passiv prosess i kroppen. EPA og DHA er aktive regulatorer som gjør at vi kommer raskere tilbake til normal tilstand.
Høsten 2013 reiser Hansen over til USA for å jobbe i laboratoriet til professor Charles N. Serhan ved Harvard Medical School.
Serhan er den som har gjort det meste av arbeidet med å vise den positive effekten omega-3-fettsyrenes metabolitter har på mennesker. Han har gjort forsøk på dyr og ett av stoffene er kommet langt i klinisk testing på mennesker.
Hansen tar med seg stoffene de har laget ved UiO, over til USA.
– Vi har brukt våre kjemikunnskaper til å lage varianter av EPA og DHA og metabolittene deres for å bekrefte Serhans funn. Når EPA oksideres uten enzymer til stede, får vi dannet ugunstig, harsknet fett. I nærvær av enzymer får vi sunne metabolitter, blant annet prostaglandiner, forklarer han.
– Vi syntetiserer og finner den kjemiske strukturen til metabolittene her ved UiO og viser at stoffene er kjemisk rene og har riktig tredimensjonal struktur. Vi kan dessuten bruke kunnskapen vår til å lage analoger som er mer stabile enn de naturlige metabolittene.
Utfordringen er å lage stoffene slik at de få en tredimensjonal struktur som er eksakt lik de naturlige metabolittene. Dette må være på plass for at analogene skal få samme biologiske aktivitet som de naturlige stoffene.
Hansen jobber med metabolitter av EPA og DHA som kalles resolviner og protektiner. Han ser spesielt på et bestemt protektin som er en metabolitt av DHA, og analoger av dette protektinet.
Det er vist at dette protektinet har effekt på inflammasjon i hjernen. Analoger av det er potensielle legemidler mot Alzheimers sykdom.
Han har dessuten studert et bestemt resolvin og analoger av dette. Det har potensielle anti-angiogenetiske egenskaper, det vil si at det kan redusere svulsters tilgang på oksygen og næringsstoffer og dermed ta knekken på dem.
Les også: Her er din nye kreftlege
Ferdige medisiner?
Dersom testingen med et stoff gir gode resultater, tar forskerne kontakt med universitetets eget kommersialiseringsselskap Inven2 som bistår med patentsøknader og å finne kommersielle samarbeidspartnere.
– For tuberkulose har ikke stoffene gitt gode nok resultater i dyreforsøk så der må vi finne nye stoffer å teste. Det er dessuten viktig å jobbe med å finne virkningsmekanismen for disse stoffene. Det kan være noe vi tar opp igjen senere, forteller Gundersen.
– Testingen av adenosinantagonistene er ikke ferdig ennå. Det finnes ulike undergrupper av adenosinreseptorer ulike steder i kroppen som alle binder adenosin, men som hver binder bare noen av analogene vi lager av adenosinantagonistene. Hvor analogene binder blir avgjørende for hva slags sykdommer vi ser på videre.
Hun legger til at de ennå ikke vet om analogene binder spesifikt nok til en bestemt undergruppe av reseptoren til at de kan gå videre med de stoffene de har nå.
Denne artikkelen er levert av Forskningsrådets kjemiprogram KOSK II (Katalyse og organisk syntetisk kjemi II).
Les også:



