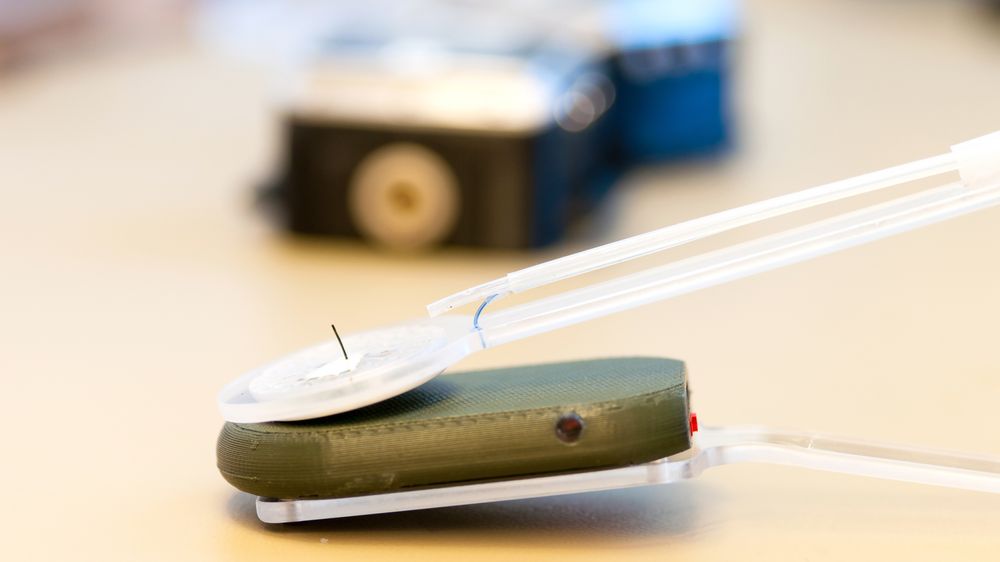
Reguleringsteknikk står helt sentralt for et forskerteam på NTNU som utvikler en kunstig bukspyttkjertel for diabetikere.
– Diabetes er i ferd med å bli en veldig teknologisk sykdom som vil øke. Det kan bli en utfordring for helsepersonell som må forstå teknologien, sier Sven M. Carlsen.
Han er professor i endokrinologi, ekspert på hormonsykdommer. Han leder et team bestående av kybernetikere, fysikere, medisinere og ingeniører der fag som elektronikk og materialteknologi står sentralt.


– Målet er å lage den perfekte kunstige bukspyttkjertel. Blodsukkeret skal ha nedre nivå 4 mmol/L og øvre nivå 8 mmol/L, diabetikere skal bli ikke-diabetikere, sier Carlsen.
Initiativet til prosjektet, kalt Artificial Pancreas Trondheim, ble tatt av postdoktor Anders Fougner, som selv er diabetiker. Fougner er utdannet ved Institutt for teknisk kybernetikk og han så at det er store reguleringstekniske utfordringer med dagens behandlinger som ikke lar seg løse med de metoder som nå brukes.
- Skal diagnostisere sykdommer via øyet: Ny skjermteknologi kan gjøre kontaktlinser til smarte biosensorer
Rett i blodbanen
Diabetes
Diabetes deles inn i to hovedtyper, type 1 og type 2. Diabetes type 1 er en insulinmangelsykdom der de insulinproduserende betacellene i bukspyttkjertelen blir angrepet og ødelagt av kroppens immunsystem. Insulin er et hormon som har en rekke funksjoner i kroppen. Den viktigste er regulering av sukker- eller glukoseinnholdet i blodet. Derfor må insulin, eller en insulinanalog, tilføres.
Diabetes type 2 er en helt annen sykdom der kroppen produserer insulin, men hvor det ikke virker tilstrekkelig godt og hvor insulinproduksjonen etter hvert blir for liten til å holde blodsukkeret i sjakk.
Den kunstige bukspyttkjertelen blir utviklet for diabetikere med type 1, men dersom prosjektet lykkes kan det også bli aktuelt å bruke samme løsning på diabetikere med type 2 som har fått behov for insulin.
Utfordringen er tid. Hos en person uten diabetes produseres og frigjøres insulin etter behov, og tilføres direkte i blodet uten forsinkelser av noe slag. Hos en diabetiker blir insulinet satt subkutant, altså i underhuden. Det gir store forsinkelser.
De samme forsinkelsene får diabetikere med de metoder som er vanlig for måling av blodsukker, hvor verdiene måles i vevsvæsken og ikke i blodet.
– Å måle og å sette insulin i huden er uforenlig med virkelig god regulering. Vi forsøkte å forstå prosessen og dynamikken. Det ideelle er å tilføre insulin rett i blodbanen mellom bukspyttkjertelen og leveren, men det går ikke på grunn av lokaliseringen i kroppen, sier Øyvind Stavdahl, førsteamanuensis på Institutt for teknisk kybernetikk.
Resultatet ble bukhulen. Der er det plass tilgjengelig, immunforsvaret er mindre aggressivt enn i andre deler av kroppen, og tidsforsinkelsene er omtrent halvert. I dag pågår det, verden rundt, en rekke forskningsprosjekter for å utvikle en kunstig bukspyttkjertel.
De fleste jobber som nå, ved å bruke underhuden. Et team i Boston jobber med bukhulen, men med noen forskjeller fra hva de gjør på NTNU.
Dagens systemer mot kunstig bukspyttkjertel:
|
|
Subkutan insulininjeksjon og måling |
Intraperitoneal insulinfusjon og måling, som teamet forsker på |
|
Tidsforsinkelse |
1.4 min |
Fra NTNUs forsøk: Snitt 9,7 sek, varierer mellom 0 og 27 sek. Mål: ˂ 10 sek. |
|
Tidskonstant |
12.4 min |
Fra NTNUs forsøk: Snitt 4.7 min, varierer mellom 0.5 og 10.2 min Mål: ˂ 1 sek˂ |
|
Maks insulinkonsentrasjon |
45 min |
15 – 25 min |
|
Maks glukosesenkende effekt |
90 – 120 min, uforutsigbar |
Foreløpig ukjent, helst under 45 min |
|
Effekt slutter etter |
5 – 6 timer |
2 – 3 timer |
|
Sensorvarighet |
6 – 8 dager |
Foreløpig ukjent, helst > 90 dager |
- Slik virker: Ultralyd og MR
Pumpe i lomma
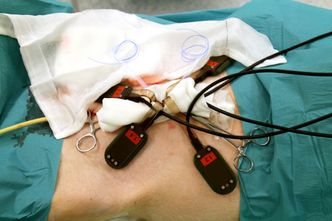
Carlsen og hans team vil operere inn en port gjennom bukveggen inn til bukhulen. Den kan stå i flere år før den må skiftes. Inn føres en slange med kombinert insulintilførsel, sensor og overføring av sensordata. Det hele styres fra en automatisk pumpe som pasienten har i lomma.


Til denne porten må de også utvikle en tett klikk-lås slik at pumpen kan koples ut før en svømmetur, for eksempel.
Dagens blodsukkermåling er hovedsakelig elektrokjemisk. Et enzym, glukoseoksidase, konverterer glukose til hydrogenperoksid, som igjen reagerer med platinaanoden i sensoren, og generer et elektrisk signal som konverteres til en blodsukkerverdi som kan leses av. Det byr på utfordringer med hensyn til varighet av sensorene fordi enzymet blir brukt opp.
Teamet på NTNU vurderer forskjellige former for optisk spektroskopi. I forsøkene benytter de en sensor levert av Prediktor Medical i Fredrikstad som bruker nærinfrarødt lys med bølgelengde rundt én mikrometer. I tillegg jobber de med å utvikle en ny egen sensor, basert på fiberoptikk kombinert med Raman- eller infrarød spektroskopi.
– Vi prøver nå ut forskjellige sensorer i bukhulen. Mitt håp er at sensoren skal vare i minst tre måneder, det gjør elektrokjemisk sensor lite sannsynlig, sier Carlsen.
- Basert på eggeskall: Et nytt plaster kan få sårene til å gro i løpet av tre uker
Kan være farlig
Ved å sette insulin i bukhulen har forskerne funnet at både tidsforsinkelsen og tidskonstanten reduseres markant i forhold til å sette insulin gjennom huden.
Enkelt forklart: Tidsforsinkelsen er tiden det tar fra insulinet er satt til det begynner å virke, mens tidskonstanten er tiden det tar fra insulinet begynner å virke til det har full virkning.
For å få redusert disse verdiene, altså for å få raskere insulinabsorpsjon, testes flere forskjellige plasseringer i bukhulen. Når det gjelder glukosemåling har teamet allerede klart å få tidsforsinkelsen ned til null på enkelte av sensorene de har prøvd.

Men det holder ikke bare å redusere tiden. Dagens sensorer reagerer på enkelte medisiner, for eksempel kan paracetamol føre til at blodsukkermåleren viser dramatisk høyere verdier enn de reelle. Det kan være farlig om en diabetiker da setter en korrigerende insulindose som det faktisk ikke er behov for.
– Vi er kjent med at dersom pasienter har en reell blodsukkerverdi på cirka 5 mmol/L (som er helt normalt, red.anm.) kan sensoren likevel vise over 20 mmol/L dersom de har brukt paracetamol. Det er livsfarlig. Vi vil se på et 30-talls potensielle interferenter fra en liste vi har fått fra USA, med testprosedyrer. Vi må forsikre oss om at sensoren ikke viser feilaktige verdier når visse medikamenter eller næringsemner brukes, i tillegg må vi se på avstanden mellom insulintilførsel og sensor og det hele må passe med hvor porten kan plasseres, sier Fougner.
- Gjør jobben der antibiotika må bite i gresset: Ninjapolymerer kan knerte multiresistente bakterier
Vellykkede forsøk
Omfang
Det er i Norge anslagsvis 28.000 personer med diabetes type 1, eller 0,6 prosent av befolkningen. Det er i overkant av 172.000 personer med diabetes type 2. Verdens helseorganisasjon, WHO, estimerte i 2014 at det er 422 millioner med diabetes på verdensbasis, men skiller ikke mellom type 1 og type 2. US National Library of Medicine, NLM, anslår at et sted mellom fem og ti prosent av disse har type 1, altså mellom 20 og 40 millioner på verdensbasis. NLM anslår også at veksten ligger mellom to og tre prosent årlig. Det er vanskelig å finne gode overslag over kostnader, men de er svært høye.
Prosjektet startet i 2013, nå er de første vellykkede dyreforsøkene gjennomført. Neste milepæl er årsskiftet 2017-18, da skal man kunne måle glukosenivå i bukhulen på en gris i åtte timer. I 2021 skal det være mulig å gjennomføre de første åtte timene på pasienter.
Prosjektet er finansiert med 24,7 millioner kroner fra Forskningsrådet og cirka 12 millioner fra Helse Midt-Norge, samt noen mindre finansieringskilder.

Før forskerne når målet er det en rekke utfordringer som må overvinnes. Den viktigste er å få blodsukkermåling som er tilstrekkelig pålitelig og robust, det vil si at den ikke bør påvirkes for mye av for eksempel kroppstemperatur, medikamenter eller bevegelser.
Den neste utfordringen blir å designe og konstruere en port som fungerer i praksis. Den tredje store utfordringen er å miniatyrisere sensorteknologien.
Men troen på at det går er sterk.
– Vi driver ikke dette som en akademisk øvelse, vi skal få frem et produkt det er behov for. Om vi ikke lykkes, er det enten fysiologiske hindringer vi ikke kommer utenom eller teknologiske hindre vi ikke kommer utenom. Teknologien finnes ikke, vi må lage den. Forskjellen på oss og øvrige forskerteam er at vi setter insulinet på et sted hvor det virker raskt, sier Stavdahl.