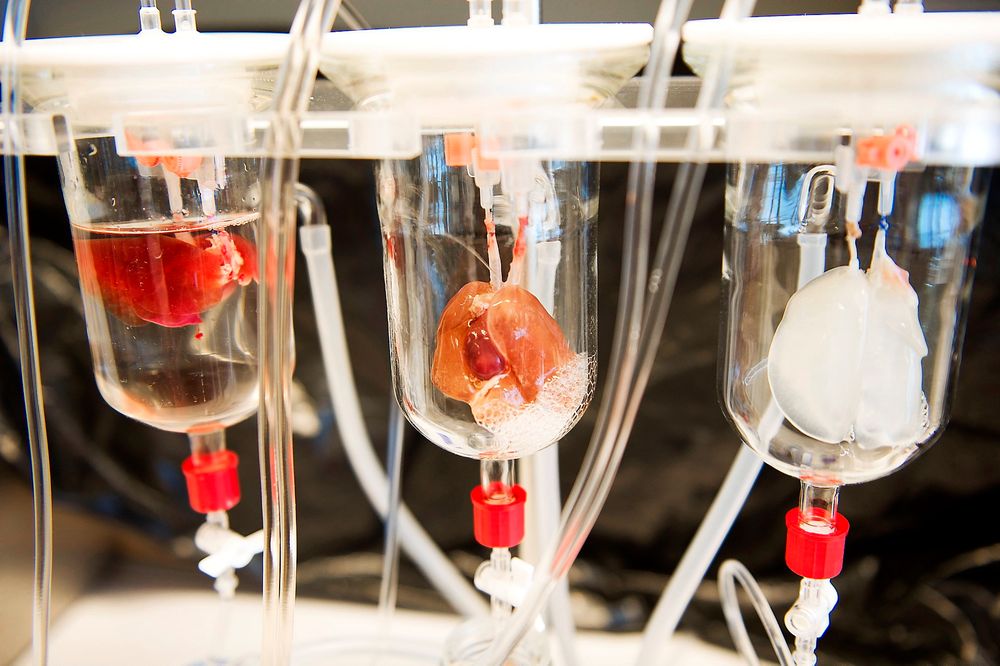
Forskningen på stamceller går på høygir over hele verden. Disse cellene kan løse svært mange helseproblemer om vi lykkes med utviklingen.
Et av de store håpene er å lage kunstige organer.
Men kunstig er kanskje ikke et helt presist ord. For slike organer vil bli bygget med pasientens egne stamceller. De vil ikke merkes som fremmed vev av immunsystemet, og de vil gjøre livet langt lettere for pasienten som slipper å gå på immundempende medisiner resten av livet.


Når vi klarer det, for det er nok mer et spørsmål om tid, vil behovet for organdonorer reduseres.
Les også: Dette plasteret kan mye mer enn å stoppe blod
Vi er i gang
– Det lages allerede enkle organer som urinblærer. Blæra er jo i praksis kuleformet, så den kan bygges på et slags stativ av en biokompatibel, porøs polymer. Tenk på den som en slags plastbasert stålull. Her kan blæreveggsceller slå seg ned slik at de danner vev som er vanntett nok til å fungere som en blære, sier lederen for Nasjonalt senter for stamcelleforskning, Joel Glover
Han forteller videre at det også «sås» ut muskelceller slik at blæreveggen får evnen til å trekke seg sammen.
– En håndfull pasienter har fått slike blærer, og her finnes det allerede noen års erfaring. De er ikke like gode som blærene vi er født med, men de fungerer, sier Glover.
Blærer er ikke det eneste som er laget. Det er bygget blodårer, og pusterøret – som har en struktur som inneholder mye brusk – er framstilt flere ganger fra biokompatible maler som er sådd ut med pasientens egne stamceller.
– Noen organer med stiv bindevevsstruktur er enklere å lage fordi vi enten kan fjerne cellene og beholde bindevevsstrukturen som er der, eller etterligne den kunstig med en polymer. Her kan 3D-printere bli en viktig teknologi i fremtiden. Tanken er å replikere organet ut fra røntgen- eller MR-informasjon og så bygge det kunstig mens pasienten ennå er i stand til å bruke sitt naturlige organ, sier Glover.
Les også: Har snudd aldringen i cellevev

Organprinter
Det å bygge organer som har lite stivt bindevev, slik som hjerte og lunger, er vesentlig vanskeligere. Det foregår spennende forskning på dette også.
3D-printere kan også her lage en slags mal av biologisk nedbrytbart materiale som så kan fylles med celler, også via printeren. Universitetet i Oslo har fått bevilget midler til å anskaffe en slik 3D-celleprinter som kan printe den trelags cellestrukturen som finnes i mange organer.
– Dette er ny teknologi som er helt i starten. Slike celleprintere må fungere etter helt spesielle kriterier. Det viktigste er tross alt at cellene er levende når de er kommet frem dit de skal være, sier Glover.
Han har stor tro på at bioprintere vil utvikle seg raskt. Mange pengesterke selskaper arbeider med å ta frem teknologien.
Les også: – Bioprinting av vev og organer vil lede til etisk debatt
.png)
.jpg)

Tømt for celler
En ny metode for å lage vanskelige organer er å benytte et donor-organ, som et hjerte fra et annet menneske, eller til og med fra et dyr, og så tømme det for levende celler. Det som da er igjen er bindevevet som nærmest er gjennomsiktig og kan brukes som et slags skjelett for nye celler.
– Dette er en svært interessant utvikling, men det er langt igjen. Vi må sørge for å plassere de riktige cellene der de skal være i en slik struktur. Et hjerte kan ikke bare inneholde muskelceller. Det er viktig at nerver og annet vev kommer på riktig sted, men denne forskningen, kombinert med 3D-skrivere for å plassere de ulike stamcellene riktig, virker lovende, sier Glover.
Les også: Nanoroboter skal behandle kreft mer effektivt enn cellegift

Innen rekkevidde
Glover tror produksjon av enkelte organer vil være etablert som en rutine utenfor forskningen i løpet av ti år.
– Selv noe så komplisert som et hjerte kan komme før vi forventer det. Det er mange grupper som arbeider med hjerter, og her ligger det mye kunnskap til grunn. Det ville ikke overraske meg om et menneske får et nytt hjerte bygget opp av sine egne stamceller før jeg går av med pensjon, sier han.
Man skulle tro at det å dyrke brusk til knær, som svært mange sliter med, ville være mye enklere. Her maner Glover til forsiktighet.
– Det er kritiske krav til slik høybelastet brusk, så det vil nok ta lengre tid enn man skulle tro før vi har fullgode prosedyrer for dette, sier han. Men det er stor forskningsaktivitet rundt dette feltet ved Universitetet i Oslo og Oslo Universitetssykehus.
Les også:
Snart kan du få behandling hos fastlegen over internett